El término medicina traslacional se acuñó en la década de 1990, pero no se usó más ampliamente hasta principios de la década del 2000. Originalmente, la investigación médica traslacional surgió a partir del concepto de «del laboratorio a la cama del paciente», como un tipo de investigación médica que buscaba eliminar las barreras entre el laboratorio y la investigación clínica.
Se puede definir la medicina traslacional como una disciplina que está avanzando rápidamente dentro de la investigación biomédica y que pretende acelerar el descubrimiento de nuevas herramientas diagnósticas y nuevos tratamientos usando un enfoque multidisciplinar altamente colaborativo. Así, la medicina traslacional traslada los últimos descubrimientos a nivel de laboratorio en estudios clínicos, e intenta responder preguntas mediante el uso de diversas técnicas de laboratorio. Su finalidad es la de mejorar la predicción, prevención, diagnóstico y el tratamiento de las enfermedades. En otras palabras, la medicina traslacional transforma los logros básicos de la investigación en teoría práctica, tecnología y métodos que concilien el laboratorio y la práctica clínica.
La medicina traslacional (figura 1) es un concepto que fluye en dos direcciones y así, promoverá el flujo de información del laboratorio a la clínica y, de la misma forma, debería promoverse de la clínica de vuelta al laboratorio.
Figura 1. Bidireccionalidad en el flujo de conocimientos que tiene lugar en la medicina traslacional
El objetivo final de la medicina traslacional es ayudar a los pacientes al permitir desarrollar nuevos métodos diagnósticos, pronósticos y la adquisición de nuevo conocimiento de utilidad en el tratamiento de enfermedades. De este modo, tanto las personas como los animales podrán tener acceso a una atención sanitaria del más alto nivel a un coste razonable.
Todavía resulta insuficiente el conocimiento de diversos aspectos biológicos fundamentales que inciden sobre la salud y enfermedad. Por ello, los hallazgos actuales aún no se pueden traducir de forma automática y totalmente fiable, en prevención y nuevos tratamientos más eficaces. Los objetivos de la medicina traslacional pueden alcanzarse únicamente mediante la inversión y los avances continuos en descubrimientos básicos biomédicos y conductuales combinados con una ciencia traslacional eficaz.
Medicina personalizada de precisión (MPP)
El riesgo de padecer una enfermedad y el modo en que el paciente responde a los tratamientos farmacológicos, están condicionados tanto por los genes como por el ambiente al que el paciente está expuesto. Este ambiente es el resultado del entorno y del estilo de vida. La integración de los datos genómicos y de otras ciencias ómicas con el conjunto de datos clínicos del paciente y de su entorno, permite adaptar la práctica clínica a las características individuales de cada paciente, en lo que se denomina MPP.
La MPP constituye una herramienta esencial para la aplicación de criterios de segmentación de la población, posibilitando adaptar las estrategias preventivas, diagnósticas y terapéuticas a las características de los pacientes. Supone, por tanto, una potente herramienta para mejorar la elección del tratamiento, evitando efectos secundarios innecesarios y racionalizando el gasto sanitario. Esto se consigue al segmentar las medidas terapéuticas en función de diversas variables (edad, sexo, raza, otras patologías, marcadores genéticos, etc.).
Los continuos y recientes descubrimientos realizados en los últimos años en el campo de la biología molecular y genética, gracias al uso de plataformas de secuenciación masiva, han permitido un avance nunca visto en la investigación biomédica. Gracias a ello, se ha ampliado en gran medida el conocimiento de las bases moleculares y genéticas de diversas enfermedades y se han podido identificar un gran número de biomarcadores que permiten establecer protocolos más precisos y ajustados al paciente, mejorando tanto su diagnóstico, pronóstico como tratamiento.
La introducción de estas nuevas técnicas de análisis, así como el tratamiento de los datos asociados, constituye un cambio de paradigma tanto a nivel de investigación, como en los modelos asistenciales, posibilitando el desarrollo de nuevos abordajes en múltiples enfermedades. Sin embargo, la aplicación generalizada de las aproximaciones que han demostrado eficacia, efectividad, seguridad y coste-efectividad, plantea importantes retos en la práctica clínica.
Ciencias ómicas en medicina veterinaria
El desarrollo de las tecnologías ómicas de alto rendimiento, como la secuenciación de genoma y exoma completo, junto con el avance de otras tecnologías ómicas (figura 2) —proteómica, metabolómica, farmacogenómica, epigenómica, transcriptómica o la microbiómica— y la posibilidad de integración de esta información con los datos clínicos del paciente, están acelerando la incorporación real de la MPP a la práctica clínica.
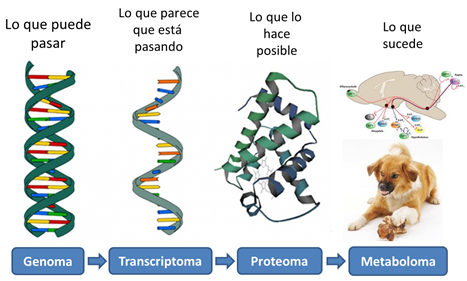
Figura 2. Ciencias ómicas más relevantes
Si bien existen numerosas publicaciones en el ámbito de las ciencias ómicas en medicina veterinaria, estas constituyen estudios aislados sin una aplicación clínica generalizada en la actualidad más allá del ámbito investigador o académico.
En los últimos 20 años se han publicado 129 artículos (figura 3) que abordan la medicina personalizada de precisión en veterinaria y muchos más en relación a patologías o técnicas diagnósticas relacionadas con la MPP. De ellos, 108 se han publicado en los últimos 5 años, lo que evidencia que la MPP no es el futuro de la medicina veterinaria sino el presente más inmediato.
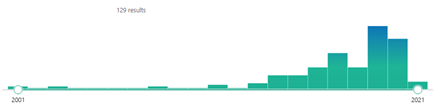
Figura 3. Evolución en el número de publicaciones científicas en materia de medicina personalizada de precisión en medicina veterinaria
Psiquiatría y etología clínica de precisión
La MPP en áreas de conocimiento como la oncología ha dado importantes frutos en los últimos años y, a día de hoy, ya es mucho más importante conocer la estirpe genética de una neoplasia que su localización. Por contra, en psiquiatría los diagnósticos todavía responden a criterios subjetivos y todavía se realiza una prescripción basada en ensayo-error.
El conocimiento de la etiopatogenia de las enfermedades mentales, a pesar de los notables progresos alcanzados, sigue siendo de «arriba a abajo», en lugar de «de abajo a arriba», lo que popularmente se conoce como «empezar la casa por el tejado». La mayor parte de los psicofármacos disponibles en la actualidad no son fruto del descubrimiento de las bases fisiopatológicas de los trastornos psiquiátricos, sino de observaciones clínicas precisas pero afortunadas, y es a partir de su mecanismo de acción que hemos deducido que algo va mal en el cerebro con la dopamina, la serotonina o el glutamato.
El DSM-5, documento de referencia en psiquiatría humana, será la última versión de la clasificación de los trastornos mentales que no incluya biomarcadores.
La psiquiatría de precisión, y por extensión la etología clínica de precisión, han llegado para quedarse, aunque todavía estén en fase embrionaria; pronto el discurso será inteligible y claro, y no será posible trabajar negando el sustrato biológico de las enfermedades mentales.
Si bien el objetivo es conseguir una medicina personalizada, en un inicio se podrán estratificar poblaciones sin alcanzar la ultradefinición individual, pero sí permitirá definir subgrupos dentro de las categorías diagnósticas. Ha ocurrido en oncología, está ocurriendo en neurología (apenas hace 10 años el diagnóstico de la esclerosis múltiple era exclusivamente clínico) y ocurrirá en el ámbito de las enfermedades mentales.
En psiquiatría y en etología clínica existen una serie de barreras ideológicas y económicas que condicionan la evolución de estas especialidades. El estigma de las enfermedades mentales todavía perdurará mucho tiempo pero las evidencias sobre la base biológica de las enfermedades mentales y la reducción de costes de biomarcadores y técnicas de secuenciación masiva abrirán la puerta de la MPP en ambas especialidades al igual que las técnicas de neuroimagen (TAC y RMN) se abrieron paso en la última década en medicina veterinaria, para ser a día de hoy técnicas de uso rutinario.
Por otro lado, como un avance transversal en todas las disciplinas médicas, la farmacogenética permite disponer de pruebas para afinar en la predicción de la tolerabilidad y respuesta a distintos tratamientos. El empleo de tratamientos que se centren en el control de los síntomas formará parte del pasado y la industria ya acepta que para descubrir nuevas moléculas con auténtico valor añadido será necesario apoyarse en la MPP, por lo que muchos fármacos ya disponen de información sobre su eficacia y tolerabilidad en pacientes con biomarcadores concretos. Si bien a día de hoy, es cierto que la sensibilidad y especificidad de los biomarcadores disponibles (genéticos, bioquímicos, electrofisiológicos, de imagen o simplemente clínicos) es insuficiente, cada vez se dispone de más información.
En la actualidad, asistimos a una auténtica eclosión de pequeñas compañías de emprendedores (start-ups) que investigan formas de validar el diagnóstico y predecir el mejor tratamiento para los enfermos mentales, también en medicina veterinaria.
Germán Quintana Diez
Doctor en Veterinaria
Máster en medicina del comportamiento y bienestar animal
Máster en Medicina genética y genómica
CEO Centro Veterinario A Marosa
CEO Wairua Genetics
Beatriz Aguiar Louzao
Grado en biología
Máster en Genética Clínica y Reproducción Asistida
CEO Wairua Genetics
Bibliografía
- Lhermie, Guillaume & Theron, Leonard & Cazer, Casey & Raboisson, Didier & Grohn, Yrjo. (2017). Veterinary precision medicine: an opportunity for cattle practitioners?. Póster en EBF conference, Bilbao, Spain, October 04th-06th.
- Lloyd KC, Khanna C, Hendricks W, Trent J, Kotlikoff M (2016). Precision medicine: an opportunity for a paradigm shift in veterinary medicine. J Am Vet Med Assoc. 248(1):45-48.
- Mealey KL, Martinez SE, Villarino NF, Court MH (2019). Personalized medicine: going to the dogs? Hum Genet. 138(5):467-481.
- Sonja Erikainen & Sarah Chan (2019). Contested futures: envisioning “Personalized,” “Stratified,” and “Precision” medicine. New Genetics and Society, 38:3, 308-330.
- Vieta E (2015). Personalised medicine applied to mental health: Precision psychiatry. Rev Psiquiatr Salud Ment. 8(3):117-8.